Desafio
Como reconhecemos se uma laranja é ácida? Que outros materiais ácidos você conhece?
Como podemos identificar se uma substância de laboratório é ácida?
Primeira Parte
Como Identificar Ácidos e Bases
Parte A - Solução de extrato de repolho roxo
Material:
- Folhas de repolho roxo
- Recipiente para aquecimento
- Fonte de aquecimento (Fogão Caseiro)
- 1 filtro de papel ou de pano
- 1 frasco grande com conta-gotas
- 1 litro de água destilada* (A água destilada pode ser encontrada em farmácias, drogarias e em lojas especializadas de produtos para automóveis, onde é vendida como água destilada bi-desmineralizada especial para baterias de carro).
- etiqueta
Procedimento:
- Pegue cinco folhas de repolho roxo e pique em pequenos pedaços.
- Coloque os pedaços de repolho roxo em um recipiente que possa ir ao fogo e acrescente água destilada até o dobro do volume ocupado pelo repolho.
- Aqueça a água com repolho, deixando ferver até que o volume se reduza à metade do volume inicial.
- Deixe esfriar e coe com um filtro.
- Coloque o extrato de repolho roxo em um frasco com conta-gotas, Rotule e conserve na geladeira.
Parte B - Testando materiais com extrato indicador
Material:
- Tubos de ensaio (10 ou mais), ou copos
- extrato indicador de repolho roxo, produzido na parte A
- conta-gotas
- materiais a serem testados, como: água de torneira, solução aquosa de cloreto de sódio, solução aquosa de açúcar, detergente líquido incolor, sabão líquido incolor, detergente para limpeza contendo amônia, vinagre branco, solução diluída de limpa-forno, suco de diferentes frutas (caju, limão, laranja, acerola, abacaxi, etc.), comprimido antiácido dissolvido em água, água sanitária, leite de magnésia e soda limonada.

Procedimento:
1) Desenhe em seu caderno uma tabela, como a apresentada abaixo, contendo uma coluna para cada um dos materiais a serem testados.
|
Material |
1 |
2 |
3 |
.... |
|
Cor inicial |
|
|
|
|
|
Cor final |
|
|
|
|
|
* Semelhante a escala Nº |
|
|
|
|
Mudanças de Cores de referência
|
Cor |
pH |
|
Vermelho |
2 |
|
Vermelho violáceo |
4 |
|
Violeta |
6 |
|
Azul violáceo |
7 |
|
Azul |
7,5 |
|
Azul esverdeado |
9 |
|
Verde azulado |
10 |
|
Verde |
12 |
2) Numere os tubos e adicione a cada um deles 5 mL de um dos materiais a serem testados, acrescente 5 mL de água e agite bem.
3) Observe e anote na sua tabela a cor inicial de cada solução.
4) Adicione 5 gotas do extrato de repolho e agite. Observe e anote a cor final de cada solução.
5) Compare as cores finais dos tubos com as cores de referência fornecidas pela tabela de referência do pH.

Destino de resíduos:
Os resíduos desta prática podem ser descartados na pia, sob água corrente!
Análise de dados:
1) Classifique os materiais testados em dois grupos.
2) Qual dos dois grupos de substâncias você considera que tem propriedades ácidas e qual apresenta propriedades básicas?
3) Com base nos testes, identifique as propriedades dos ácidos e das bases em contato com indicadores ácido-base (no caso o extrato de repolho roxo).
4) Quais materiais são mais ácidos e quais são mais básicos? Justifique.
5) Qualquer material ácido ou alcalino (básico) é prejudicial a saúde? Por que?
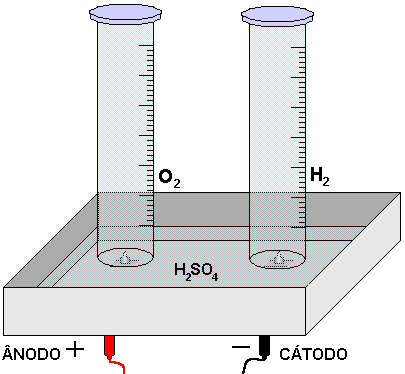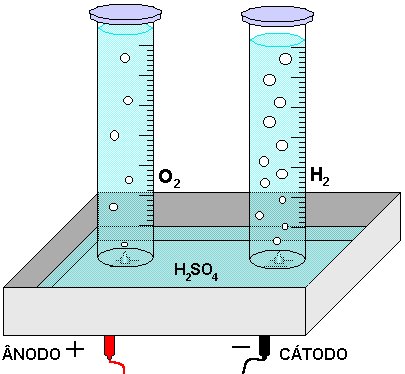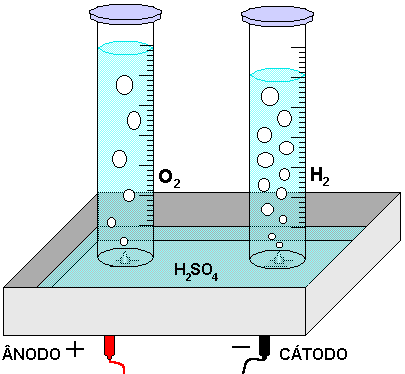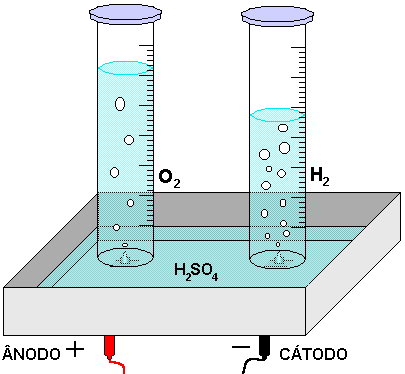
O que acontece quando corrente elétrica passa por um líquido?
O que você entende por eletrólise?
Segunda Parte
Eletrólise do Iodeto de Potássio (ou Eletrólise do Cloreto de Sódio)
Material:
- Fonte de alimentação de corrente contínua (sequência de 4 pilhas grandes ou bateria de 9 volts)
- 1 rolo de Fita Isolante
- 2 barras de grafite (de um lápis, por exemplo) de 7 cm de comprimento, cada uma, como eletrodos*
*Preparo do eletrodo de grafite: Enrole em uma das extremidades de um bastão de grafite, com aproximadamente 7 cm de comprimento, um cabo flexível de cobre de 1,5 mm2 com 30 cm de comprimento e desencapado em ambas as extremidades, dê 3 voltas, em seguida isole a ligação com um pedaço de Fita Isolante .
- 2 pedaços de cabo flexível de 1,5 mm2 de 30 cm, cada um, para as conexões elétricas
- 2 béqueres de 250 mL
- 1 litro de água destilada* (A água destilada pode ser encontrada em farmácias, drogarias e em lojas especializadas de produtos para automóveis, onde é vendida como água destilada bi-desmineralizada especial para baterias de carro).
- solução de KI (iodeto de potássio) a 5 %, conhecida comercialmente como Lugol 5,0 % - Iodo Inorgânico (10 g de sal em 200 mL de água); se não houver KI pode-se utilizar NaCl, cloreto de sódio, o sal de cozinha comum, nas mesmas proporções, ou seja, 10 gramas de sal em 200 mL de água.
- solução saturada de amido (somente se estiver utilizando solução de KI)
- solução de extrato de repolho roxo
.jpg)
- Pegue cinco folhas de repolho roxo e pique em pequenos pedaços.
- Coloque os pedaços de repolho roxo em um recipiente que possa ir ao fogo e acrescente água destilada até o dobro do volume ocupado pelo repolho.
- Aqueça a água com repolho, deixando ferver até que o volume se reduza à metade do volume inicial.
- Deixe esfriar e coe com um filtro.
- Coloque o extrato de repolho roxo em um frasco com conta-gotas, Rotule e conserve na geladeira.
- Introduza os eletrodos de grafite dentro do béquer de 250 mL, tomando o cuidado para não deixar os eletrodos de grafite se tocarem.
-
Conecte os cabos flexíveis na fonte de corrente contínua.
-
Coloque água destilada até 2/3 do volume do béquer, pingue cinco gotas de extrato de repolho roxo e cinco de amido (somente se estiver usando solução de KI) e observe por cinco minutos.
-
Troque de béquer, colocando no segundo, a solução de KI. Depois pingue cinco gotas de extrato de repolho roxo e cinco de amido (somente se estiver usando solução de KI) e observe por cinco minutos.
Destino de resíduos:
Os resíduos desta prática podem ser descartados na pia, sob água corrente!
Análise de dados:
- O que você observou ao passar corrente elétrica pelo béquer contendo água destilada?
- Quais os íons presentes na solução? Quais serão atraídos para o polo negativo e quais serão atraídos para o polo positivo?
- Qual o objetivo do extrato de repolho roxo - indicador ácido/base - no experimento? O que podemos afirmar com base em seu efeito?
- A solução de KI contém iguais quantidades de íons H+ e OH-. Como podemos relacionar o efeito do extrato de repolho roxo com essa informação? Proponha uma semirreação que justifique essa hipótese.
- O amido indica a presença de iodo (I2), conferindo coloração violeta à solução. De acordo com o experimento, de onde pode ter surgido o iodo? Proponha uma semirreação que justifique essa hipótese.*
- Caso você utilize a solução de cloreto de sódio (NaCl), explique quais as cores que você observou que apareceram ao redor do anodo (pólo positivo) e do catodo (pólo negativo) durante a eletrólise.
- Faria diferença se ao invés de utilizarmos um eletrodo de grafite, nós utilizássemos um eletrodo de cobre para realizar a eletrólise do iodeto de potássio (ou cloreto de sódio)? E um eletrodo de zinco? Explique detalhadamente seu raciocínio.